化学学科生态文明教育专题·教学设计(一)——《硫和氮的氧化物》
《硫和氮的氧化物》教案
宜州区第一中学 化学组
1.1了解SO2、NO、NO2的物理性质,掌握其化学性质。
1.2掌握氮氧化物之间的转化
1.3了解SO2、NO、NO2对空气的污染及其防治。
通过交流研讨、观察、思考等过程训练科学的学习方法
3.1通过对硫酸型酸雨与硝酸型酸雨等环境污染产生的原因和如何保护环境等问题的探讨,感受保护环境的重要性从而激发学习兴趣。
3.2通过对生产、生活实例的分析,体验化学是源于生产、生活的,并且服务于生产、生活。
3.3培养学生辩证认识事物两面性的哲学观点。
1.通过第四章前两节的学习,学生已对非金属元素有了一定的认识和了解,对元素化合物的知识也有了一个整体思路。
2.具有氧化还原反应的相关知识,能从氧化还原角度去分析简单的化学反应。
3.本节课所涉及的漂白、酸雨等知识贴近日常生产生活,学生容易接受。
4.本节课的学习有助于学生关注生活,用所学的化学知识解决身边的问题,解释生活中的现象。
5.高一年级的学生年龄一般在15岁左右,思维敏捷、活跃,但不够严谨。比较喜欢动手做实验,但缺乏正确的科学探究方法。因此,必须在实验探究活动中加以培养勇于大胆实践、创新的精神。此外,在前面的教学中,已尝试过许多的探究或验证实验,学生已经具备了一定的动手能力,能够胜任本节课的实验探究活动。
三、教学重点
1、SO2的化学性质
NO、NO2的产生及两者的转化,NO2与水的反应
1、通过实验探究,理解SO2的漂白性
2、NO、NO2的产生及两者的转化,NO2与水的反应
(1)了解SO2的物理性质,掌握它的化学性质。
(2)丰富对+4价硫元素的化学性质的认识。
(3)了解SO2对空气的污染及其防治
(1)通过实验,进一步提升基本的化学实验技能。
(2)运用实验的方法学习二氧化硫的主要性质,学会获取知识的方法;
(3)提高实验观察、分析推理及书写表达能力。
(1)通过对酸雨等环境污染产生的原因和如何保护环境等问题的探讨,感
受保护环境的重要性从而激发学习兴趣。
(2)通过对生产、生活实例的分析,体验化学是源于生产、生活的,并且
服务于生产、生活。
(3)培养学生辩证认识事物两面性的哲学观点。
重点:SO2的化学性质:氧化性,还原性,漂白性
难点:通过实验探究,理解SO2的漂白性
3、课前准备:二氧化硫气体若干瓶,玫瑰花,溴水,澄清石灰水,
氢氧化钠溶液,品红溶液,试管,导气管
在预先准备好一个化妆瓶中将玫瑰花伸入其中,看一下化妆后的玫瑰是不是变的更漂亮了呢?
设计意图:激起学生的兴趣,引导学生一起来研究这位神奇的化妆师——二氧化硫。并展示当天的天气预报,进一步引起学生的注意。
1、指导观察:学生观察已制取的SO2气体的颜色、闻气味,与空气密度比较。
2、设计实验:证明二氧化硫能溶于水。
将SO2气体通入到蒸流水中,滴加几滴石蕊试液,用试纸测定其溶液的PH。
〔教师引导〕要求学生观察现象,分析原因并得出结论。引导学生得出二氧化硫与水反应生成亚硫酸。
3、引导小结:学生小结二氧化硫的颜色、气味、状态、沸点、密度、溶解性等物理性质。
『设计意图』 通过上述“滴有紫色石蕊试液后,溶液变红。”这一现象,得出结论: SO2溶于水后形成的溶液显酸性。通过引导学生分析其原因,引出“二氧化硫的化学性质”的新课;引出“二氧化硫与水的反应”这一化学性质。
【投 影】思考问题:
1、思考SO2是什么氧化物,具有哪些性质?
2、S元素有哪些常见化合价?
3、从以上方面预见一下SO2 可能具有的化学性质,并说出理由。
4、设计实验证明SO2可能具有的化学性质(我们这里准备了石蕊试液,新制H2S溶液,酸性KMnO4溶液,溴水,品红溶液,氢氧化钡溶液等溶液。)
〔学生讨论〕由化学式可以看出,SO2中S处于中间价态+4价,所以SO2既有氧化性又有还原性。二氧化硫可能具有酸性氧化物的通性,氧化性和还原性。同时它又是一种独一无二的化学物质,理应还具有它自己的一些“小个性”。
①二氧化硫与水的反应
〔教师引导1〕类比CO2与水的反应,类比 H2CO3,引导学生写方程式,并强调其中的可逆符号。引导学生说出H2SO3的性质,如具有酸的通性,能与碱反应等。由此总结SO2也是一种酸性氧化物,化学性质与CO2相似。
②二氧化硫与碱的反应
〔教师引导〕根据二氧化硫的物质分类判断它可能是酸性氧化物,具有酸性氧化物的通性。SO2是酸酐,酸性氧化物,怎样设计实验证明?
〔学生回答〕通过与碱反应来证明二氧化硫是酸性氧化物。
【学生实验】由学生SO2通入澄清的石灰水,据现象总结出:SO2也可使澄清的石灰水变浑。同时澄清初中时的一个局限性认识:能使澄清石灰水变浑浊的气体不仅有CO2还有SO2。这将有利于学生对元素化合物知识体系网络化的形成。
⑵ SO2的氧化、还原性(以化合价为主线探究SO2可能具有的性质)
①弱氧化性
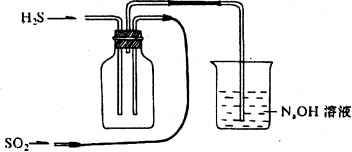 【学生实验】
【学生实验】
〔讨论交流〕通过观察SO2和H2S反应的实验现象,并结合氧化还原反应的规律推测SO2和H2S反应的生成物,尝试写出反应的化学方程式,并分析电子转移情况。
『设计意图』 利用氧化还原规律分析二氧化硫与硫化氢的反应的产物,推出二氧化硫具有氧化性。培养学生分析问题能力。
②较强还原性
【学生实验】将SO2气体通入到溴水溶液中,观察溴水的颜色变化?
【投 影】Br2+2H2O+SO2 → 2HBr+H2SO4
〔教师引导〕引导学生用电子得失的观点分析用单桥法标出电子转移的方向和数目,并指出氧化剂、还原剂。
【投 影】思考问题:
1、从化合价角度分析此反应体现氧化性还是还原性?
2、该反应的条件及特点?
【投影总结】SO2也能被其它卤素单质氧化,还能使酸性高锰酸钾溶液褪色,并且能被氧气氧化,但需要一定的条件。在加热和有催化剂的作用下,SO2被氧化为SO3,在相同条件下,SO3又部分分解生成SO2和O2,因此,该反应也是可逆反应。现有氢硫酸(H2S)、 H2O2和KMnO4三种溶液,要设计实验证明二氧化硫有还原性该如何选择?
『设计意图』 精心设计自学指导提纲,使学生的思考更全面更深入,对把握二氧化硫的还原性起到积极的作用。
【PPT】①你知道银耳原本是什么颜色的吗?为何市场上销售的银耳是白色
的,它们是如何做成的吗?②这体现了SO2的什么性质?
〔推 测〕SO2具有漂白性
【演示实验】二氧化硫漂白品红溶液。
2、【投 影】提供实例:为什么长时间放置的报纸和草帽会变黄?
【引导学生总结】:SO2溶于水生成了亚硫酸,亚硫酸跟有色物质结合生成一种无色的不稳定的化合物。加热时,或放置长时间后,无色的不稳定化合物分解释放出SO2,溶液又会恢复原来的颜色,因此,SO2的漂白作用是不能持久的。
请学生填以下表格:比较二氧化硫和氯水的漂白性
名 称 | 二氧化硫 | 氯 水 |
漂白原理 | ||
反应实质 | ||
漂白效果 | ||
漂白范围 |
【学以致用】1.一瓶品红溶液通入某种气体后褪色,通入的气体可能是什么?如何设计通入气体的成分?2.如何鉴别CO2和SO2 ?
〔自学指导〕从二氧化硫的性质出发,研究它的实际应用。
【投 影】二氧化硫的用途(学生归纳后投影)
【图片展示】⑴制造硫酸
⑵可以漂白白纸浆、毛、丝、草编制品等。
⑶杀灭霉菌和细菌作食物和干果的防腐剂。
『设计意图』 用辩证的观点分析问题,明白任何事物的性质都是一分为二的,有些能带来用途,有些能带来危害。
【投 影】展示被酸雨侵蚀的植物照片,被酸雨腐蚀前后的石雕像的对比照片,让学生感受酸雨对人类生存环境带来的危害,让学生真切地体会到地球面临的严峻考验和全球环保的重要性。引起学生的心灵的震撼,从而激发环保意识。并分组讨论怎样减少大气中SO2含量?(学生交流后投影)
【投 影】二氧化硫污染的防治方法
1、改善燃料种类,积极开发新能源
2、固硫。如煤中加入钙基(CaO)
固硫原理为:CaO+SO2=CaSO3 2CaSO3+O2=2CaSO4
3、种植能够吸收SO2的有关树木(如臭椿、垂柳、柳杉)等
4、有效直接利用。用Na2SO3吸收SO2,又利用NaHSO3分解产生高浓度的SO2,作为制取硫酸的原料
5、提高全民环保意识。
『设计意图』 让学生将所学的知识应用到实际生活中,感受化学学科的价值。
评 价:
学生积极的投入交流、讨论中并进行总结。整体的思路清晰,问题回答的比较到位。就是有点小吵。
使学生整体把握本节主要学习内容并进行小结:本节课我学到了什么?学会了哪些化学知识和学习方法,还存在哪些学习上的困惑,对老师的教学方法有哪些建议。
【投 影】1、能够用于鉴别SO2和CO2的溶液是( )
A.澄清的石灰水 B.品红溶液
C.紫色石蕊试液 D.氯化钡溶液
2、为了除去混在CO2气体中的SO2和O2气,以下试剂:①饱和Na2CO3溶液;②饱和NaHCO3溶液;③浓H2SO4;④灼热铜网;⑤碱石灰,使用顺序正确的是( )
A.①③④ B.②③④ C. ③④⑤ D.②④③
3、酸雨的形成主要是由于( )
A.大气中二氧化碳含量增多 B.汽车排出大量尾气
C.工业上大量燃烧含硫燃料 D.森林遭乱砍滥伐,破坏了生态平衡
4、下列反应中,SO2表现氧化性的是( )
A.2SO2+O2=2SO3 B.SO2+H2O=H2SO3
C.SO2+2H2O+Cl2=H2SO4+2HCl D.2H2S+SO2=2H2O+3S



 微信收款码
微信收款码 支付宝收款码
支付宝收款码